
東工大は 抗ウイルス薬アラセナの発祥の地
ビタミンB2からウルソへと続く伝統が 更にアラセナへ繋がった
長い間ウイルスに効く薬はできないだろうと考えられていた。この壁を打ち破る画期的な薬(アシクロビル,DNA合成酵素の阻害剤)が1974年に米国の製薬会社で開発され,1988年にノーベル賞に輝いた。本学のビタミン研でも抗ウイルス薬の開発を可能にする画期的な有機合成反応が開発されていたと知って調べてみた。
抗ヘルペス薬
最近話題のタミフルのお陰で,抗ウイルス薬は子供たちの会話にも登場するほど有名になっている。ここで紹介する抗ウイルス薬アラセナ(9-β-D-アラビノフラノシルアデニン;ara-A)は アシクロビルと似た働きをし ヘルペスウイルスの増殖を抑えるが,タミフル(シアル酸類似体)とは作用機構が異なるためにインフルエンザウイルスには効かない。タミフルが,インフルエンザの特効薬として,世に出たのは ちょうど世紀の変わり目の2000年前後だったのに比べ,ここで紹介する“東工大 & 味の素版”抗ウイルス薬アラセナが生まれたのは1984年で,抗ウイルス薬の草分けの一つだった。30年たった今も盛んに処方されている。
稀にみる理想的な結果
1960年代後半にara-A(図1の❸)が抗ウイルス薬になる可能性が示されたが1,2),生命に欠かせないリボヌクレオシドの一種であるアデノシン(図1の❹)の水酸基(OH)の向きを1ヶ所だけ反対方向に変えたのがara-Aである。
これを工業的規模で合成することは,当時の科学技術では,常識的に不可能だった。実際,ノーベル賞を取ったクループも,ara-Aに触発されたが合成したのはより簡単な誘導体ばかりで,その中に幸運にもアシクロビルが含まれていた。
我が東工大グループは,常識にとらわれず,この水酸基の“向き変え”に成功した3)。
図1に示すように,混ぜて熱をかけるだけで欲しいものを手に入れたのだから素晴らしい。しかも高収率で副産物はほとんど生成しないという理想的な結果だった。ホスゲン(神経毒)を使わないで,安定な炭酸エチレンを用いて環状炭酸エステルの交換を実現した点でも画期的だった。思わず「オーイ,いっちゃったよ!」と叫んだそうだ。
この反応が生まれた場所も特筆に値する。その場所はビタミンB2の合成で世界的に有名になっており,ビタミン研と呼ばれていた。ビタミンB2の合成が優れた若手を惹きつけ,抗ウイルス薬の開発につながる研究の基礎を築いたという意味で,科学研究における伝統と名声の大切さを物語っている。
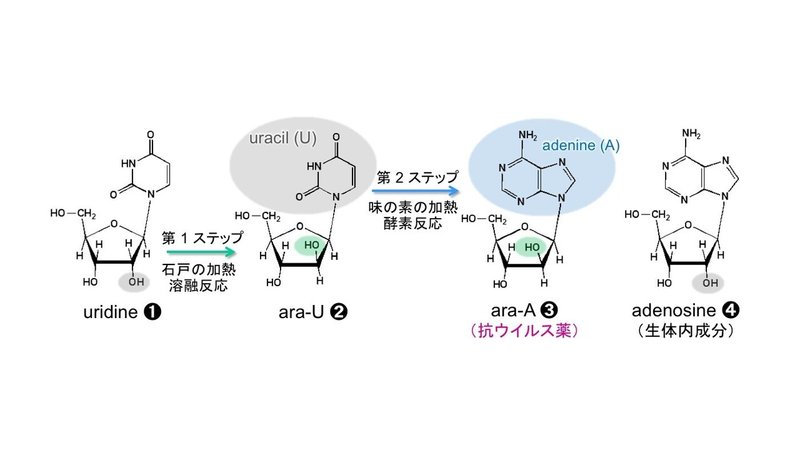
図1 アラセナ(ara-A)の構造を合成過程
ビタミン研の伝統
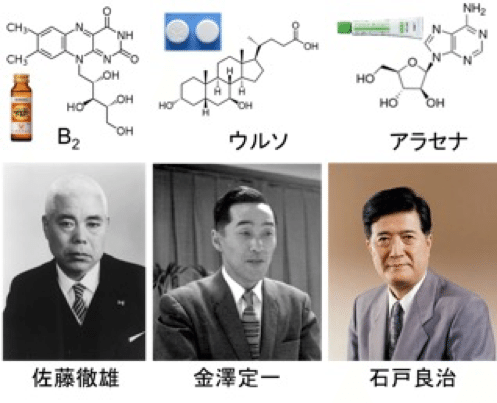
この物語の中心人物である石戸良治は薬学を勉強した後,ビタミンB2合成のリーダーだった佐藤徹雄(1908~1968)の門をたたいた(研究生;1956)。
「君はヌクレオシドをやりたまえ」という佐藤の一言で方向は決まったが,何をどうすればいいかは暗中模索だった。そんな時に参考になったのが,佐藤の片腕としてビタミンB2合成に取り組んだ渡部憲治(1951年没,32歳)や,ビタミンB2の次に佐藤研究室が取り組んだ「熊胆(くまのい)」の薬効成分4)(ウルソ)の合成と工業化の際に中心的な役割を果たした金沢定一(2006年没,81歳)らの実験に対する真摯な姿だった。
彼らの活躍は語り草になっていた。こうしたビタミン研の雰囲気が石戸を薬剤師から科学者へと変身させていった。
鍵となった 炭酸エステルを用いる合成研究
石戸が,佐藤の助言もあって,ヌクレオシドに関する研究に着手して間もなくのことだった。リボヌクレオシドの一種であるウリジンを炭酸エチレンと加熱・溶融すると,他のポリヒドロキシ化合物と同様,いとも簡単に環状炭酸エステルの交換反応が起こり,更に幸いなことには,炭酸ガスの副生を伴って分子内環化反応までが起こり,水酸基の向きが反対のanhydro-ara-Uだけが得られることを見つけた3)。
これを酸加水分解すれば,容易にara-Uが得られる(図1の第1ステップ)。炭酸エチレンは安価で,しかも反応も収率よく進行する。工業化には理想的な方法だ。これに目を付けた「味の素」は,生体触媒といわれる酵素を利用してara-Uの糖部をそのまま核酸塩基アデニンに転移(グリコシル基転移)させ,抗ウイルス作用を有するara-Aの合成に成功している5)。
安価な試薬,合成過程の単純さ,及び収率の良さから,30年を経た今もヘルペスウイルス(DNAウイルス)によって引き起こされる口内炎等の治療に欠かせない薬として広く使われている。
水酸基(OH)の向きが1ヶ所異なるだけで,これだけ有効な薬になることも驚きだが,通常の有機化学反応と違って,反応部位以外の官能基に保護基を予め導入することなく,しかも当時常套手段となっていた毒ガス・ホスゲンを使わず,環状炭酸エステルの交換反応を軸にanhydro-ara-Uの合成を実現し,水酸基の向きを変えることに成功した実験も見事というしかない。
ポロネーズ

石戸はショパン音楽の愛好家だ。ショパンといえば「英雄ポロネーズ」を思い浮かべる人も多いだろう。ポーランドが生んだ天才音楽家で,よく「ピアノの詩人」と評される。祖国の民謡のリズム(ポロネーズ)を取り入れて作られたのが かの名曲「英雄ポロネーズ」だ。
ビタミンB2や肝機能改善薬ウルソの研究の延長線上で,それらに共通な基調(リズム)を精神的支えにして生み出された抗ウイルス薬ara-A(商品名:アラセナA,アラセナS)は,まさしく「東工大のポロネーズ」といえよう。口内炎や帯状疱疹でアラセナの世話になったら東工大を思い出し,宣伝して頂きたい。
執念の発見---災いを福とした観察力と洞察力

第二ステップは,酵素の力を借りてara-Uの糖部をアデニン(A)に転移させる反応である。こういうと簡単そうであるが,実際には苦労の末にようやく実現し,「執念の発見物語」として語り継がれている6)。
味の素では,化学合成グループが,第一ステップは石戸らの反応を使うことにし,第二ステップの戦略を練っていた。ちょうどそこへ,核酸醗酵グループが入ってきて,微生物の持つ酵素で何とかしようということになった。
化学合成グループが供給してくれるara-U(図1の❷)とアデニンを原料とし,核酸醗酵グループがara-Uの糖部をAに転移させ,ara-A(図1の❸)を産生してくれる微生物を探すのだが,なかなか見つからない。どうも反応系にせっかく加えたアデニンが脱アミノ化されたヒポキサンチン(Hx)しかできていないようだ。一年以上も悪戦苦闘していた。
微生物の酵素を利用して有機合成を行うには,微生物から取り出した純粋な酵素を使うのが理想的だが,生産コストを考えると微生物をそのまま使いたい。しかし,その場合はデメリットもある;微生物の中には多くの酵素が含まれており,必ずしも望む酵素のみが働いてくれるとは限らず,時には困った副反応が進行してプロジェクトが暗礁に乗り上げてしまうからだ。ara-Aプロジェクトの場合は,サーモスタットの故障のお陰で,ブレークスルーがもたらされた。
ある朝,反応槽から湯気が出ているのを見て担当者は驚いた。普通の酵素は熱に弱いので,反応槽は30℃にセットしてある。サーモスタットが故障し,温度が60℃にも上昇してしまっていたのだ。
事故にならなくてよかったと胸をなでおろしながら,サンプルを捨てようとして,結晶が出ていることに気付いた。分析してみると,なんとara-Hx(ara-ヒポキサンチン)ではないか。それならば,酵素反応としては非常識だが最初から高温でやってみよう。
こうして,ara-Uの糖部をAに転移させる微生物が見つかった。この微生物に含まれるグリコシル基転移酵素は60℃で安定だが,アデニンを分解する酵素(デアミナーゼ,副反応の元凶)は熱に弱く,60℃で失活することが判り,第二ステップも温度を上げることによりクリアーできた。
当然,この酵素反応も可逆であるが,ara-Aの優れた結晶性が幸いして,反応が圧倒的に右向きに進むことも確認された。第一,第二の両ステップ共に簡単で収率がよく,今も工業的スケールで合成され,抗ウイルス薬として無くてはならない存在となっている。特に,アシクロビルが効かないヘルペス性脳炎の治療には欠かせない。産学共同の見事な成果といえよう。
今も全く同じ原理で稼働するara-Aの生産ライン
ara-Aが,アラセナという名で,世に出たのが1984年。それから30年以上経た今でも,その製造法は変わっていない。難しい反応を,安価な原料から出発して,いかに少ないステップ かつ高収率で実現するかは有機化学者の腕の見せ所であるが,ara-A合成の場合はこの3条件が完璧なまでに揃っている。

石戸夫妻らによるara-A(アラセナ)生産プラントの見学
味の素㈱東海事業所,2014年5月
白衣姿 左から:石戸雅子,小村 啓(東工大時代の石戸の教え子で1973年の論文の筆頭著者),石戸良治。
作業着姿 左から: 船越 直(製造部汎用プラント課長),片岡範康(東京薬科大学時代の石戸の教え子)。
参考文献
1) de Rudder J, Privat de Garilhe M. Antimicrobial Agents and Chemotherapy, 5, 578–584 (1965).
2) Miller FA et al. Antimicrobial Agents and Chemotherapy, 8, 136–147 (1968).
3) Komura H, Yoshino T, Ishido Y. Bull. Chem. Soc. Jpn., 46, 550–553 (1973).
4) 橋本 弘信“小粒でピリリ東工大の発明品ウルソ”東工大クロニクルNo. 349, 4–5 (2000).
5) Utagawa T et al. FEBS Lett. 109, 261–263 (1980).
6) 井澤 邦輔“執念の発見物語”医薬品のプロセス化学(第2版),化学同人,62頁 (2012).
アラセナ = ビダラビン (Vidarabine)
アシクロビル = ゾビラックス
2013年9月(初版)
2021年6月(web版)
(発行) 東京工業大学 博物館 資史料館部門

